Acne: il Roaccutan efficace ma associato a gravi effetti indesiderati
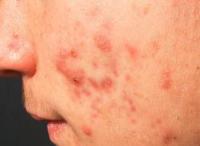

20 AGOSTO 2013 - Non sono pochi, i giovani che hanno problemi di acne, spesso in forma acuta. Per il trattamento di questa patologia, vi sono numerosi farmaci, ma l’Isotretinoina (acido-cis-13-retinoico), in Italia commercializzata con il nome di Roaccutan (Accutane negli Stati Uniti), è quello attualmente più potente, oggi disponibile, per il trattamento della forma grave di acne.
Un ciclo di trattamento con Isotretinoina della durata di 5 mesi permette una remissione prolungata dell’acne in più dell’85% dei pazienti. Alcuni pazienti possono richiedere più di 1 ciclo di trattamento. Il farmaco in questione, secondo quanto è dato apprendere da alcune ricerche, presenta alcune controindicazioni che è sempre opportuno conoscere prima d’iniziare il trattamento.
Tra i rischi, è noto che può causare aborto e gravi difetti al nascituro. Inoltre, i pazienti che assumono il farmaco possono incorrere in gravi problemi che interessano un certo numero di organi, tra cui il fegato, l’intestino, gli occhi, il naso e l’apparato scheletrico.
Poiché l’Isotretinoina è un farmaco ad alto rischio il suo impiego dovrebbe essere riservato ai casi di acne cistica recalcitrante grave.
Questo tipo di acne è resistente al trattamento standard, tra cui gli antibiotici, ed è caratterizzata da molte lesioni infiammatorie nodulari e cistiche piene di pus.
Queste lesioni possono causare dolore, cicatrici permanenti ed effetti psicologici negativi.
L’FDA (Food and Drug Administration), l’afenzia federale statunitense che vigila sui farmaci, ha approvato l’Isotretinoina nel 1982 e, da allora, quasi 5 milioni di americani e 12 milioni nel mondo sono state trattati con Isotretinoina, secondo i dati forniti dalla casa produttrice Roche.
La metà delle persone che assumono il farmaco sono di sesso femminile, la maggior parte delle quali è in età fertile ( 15-44 anni ).
Il rischio di difetti alla nascita tra le donne che assumono l’Isotretinoina è estremamente alto.
Questi difetti comprendono idrocefalia e microcefalia, difetti cardiaci, deformità facciali, come labbra leporine e orecchie mancanti, e ritardo mentale.
Dati di letteratura indicano che il 5-35% dei feti esposti all’Isotretinoina andranno incontro ad una malformazione.
Nonostante nella scheda tecnica del prodotto fosse indicata la tossicità fetale, diverse segnalazioni di gravi difetti alla nascita sono giunte subito dopo la commercializzazione del farmaco.
Allo scopo di ridurre l’uso del farmaco in donne fecondate, la società produttrice Roche, nel 1988, diede vita al Programma PPP (Pregnacy Prevention Program), in italiano Programma di Prevenzione della Gravidanza, per educare ulteriormente le donne ed i medici ad evitare i casi di tossicità fetale.
Alle donne in età fertile che assumevano Isotretinoina veniva anche consigliato di seguire un programma anticoncezionale un mese prima, durante, ed un mese dopo il trattamento.
Tuttavia, il Programma PPP non è riuscito ad eliminare del tutto le gravidanze in donne che stavano assumendo l’Isotretinoina.
Nel 2005, è stato approvato il Programma iPLEDGE con maggiori restrizioni. iPLEDGE permette di ricevere una confezione di Isotretinoina solo se le donne vengono registrate in questo programma elettronico.
Al di la di questi aspetti più noti e pertanto oggetto di maggiore attenzione da parte dei soggetti, in particolare donne che l’assumono, e dei sanitari che la prescrivono, vi sono altre avvertenze sulle quali lo “Sportello dei Diritti”, vuole porre l’accento per ricordare che questo farmaco deve essere prescritto solamente da o sotto la supervisione di medici che abbiano esperienza nell’uso dei retinoidi sistemici per il trattamento dell’acne grave e che comprendano pienamente il rischio del trattamento con isotretinoina e la necessità di monitoraggio.
Infatti, in alcuni pazienti, l’assunzione dell’Isotretinoina è associata a gravi disturbi psichiatrici.
Nonostante che la depressione fosse inserita nella scheda tecnica di prodotto, l’FDA nel 1998 ha ritenuto opportuno ri-sottolineare il pericolo di gravi disturbi psichiatrici nel corso del trattamento con Isotretinoina.
Nella scheda tecnica è stata inserita l’avvertenza che l’assunzione di Isotretinoina può produrre depressione e psicosi, e che in rari casi il paziente può andare incontro ad ideazione suicidaria, tentativi di suicidio e suicidio. Tuttavia la relazione tra Isotretinoina e depressione non è stata scientificamente dimostrata. È ovvio, infatti, che alcuni pazienti, all’atto di assumere l’Isotretinoina, potrebbero già soffrire di depressione.
Come detto, il farmaco in questione viene utilizzano per la cura di forme severe di acne nodulare recalcitrante. Tuttavia, la pubblicazione di alcuni case-report e la segnalazione spontanea di reazioni avverse hanno suggerito un'associazione tra isotretinoina, depressione e comportamenti suicidari, anche se gli studi effettuati hanno fornito risultati contrastanti.
Quindi, in tal senso, è opportuno riportare un'ampia sintesi di una ricerca pubblicata sul British Medical Journal.
In questo studio sono stati presi in considerazione pazienti trattati con isotretinoina per l'acne grave tra il 1980 e il 1990 e di età compresa tra 15 e 49 anni al momento della prima prescrizione. I dati sono stati collegati a quelli dei registri dei ricoveri ospedalieri e di mortalità (1980-2001).
Nel corso dello studio è stato effettuato, in 3 diverse finestre temporali (prima, durante e dopo il trattamento), un confronto tra il tasso di tentati suicidi nel gruppo preso in esame e quello nella popolazione generale utilizzando il registro nazionale dei ricoveri ospedalieri. I dati sono stati stratificati per sesso, 5 fasce di età e per anno di calendario allo scopo di calcolare il numero atteso di eventi nella popolazione in studio in ciascuna finestra temporale.
L'outcome principale era rappresentato dal tasso di incidenza standardizzato (calcolato dal rapporto tra numero di tentati suicidi osservati e numero di eventi attesi standardizzati per sesso, età ed anno) calcolato a partire dai 3 anni precedenti, durante e fino a 15 anni dopo la fine del trattamento.
Sono stati esaminati 5.756 pazienti di cui il 63% di sesso maschile. L'età media per gli uomini era di 22,3 anni, mentre per le donne era 27,1 anni. La durata media del trattamento era di 6 mesi per gli uomini (durata totale 1.819 anni-persona) e 6,1 mesi per le donne (durata totale 1.091 anni-persona). Oltre il 90% dei pazienti ha ricevuto un solo ciclo di trattamento.
Tra il 1980 e il 2001, il 2,2% dei pazienti (1,9% degli uomini; 2,7% delle donne) è stato ricoverato almeno una volta per tentato suicidio, per un totale di 210 ricoveri registrati (1,6 per persona).
Il tasso di incidenza standardizzato, ricavato confrontando il gruppo in esame con la popolazione generale, è aumentato gradualmente per il primo tentativo di suicidio da 0,89 (IC 95% 0,54-1,37) nei 3 anni prima del trattamento a 1,36 (0,65-2,50) nell'anno precedente il trattamento del primo tentato suicidio e da 0,99 (0,65-1,44) nei 3 anni prima del trattamento a 1,57 (0,86-2,63) nell'anno precedente il trattamento per tutti i tentativi.
Il rischio è risultato maggiore nei 6 mesi successivi all'inizio del trattamento: 1,93 (1,08-3,18) per il primo tentativo e 1,78 (1,04-2,85) per tutti i tentativi. Infine, è stata osservata una diminuzione del tasso di incidenza standardizzato nei 3 anni successivi al trattamento: 0,97(0,64-1,40) per i primi tentativi e 1,04 (0,74-1,43) per tutti i tentativi.
Non è stata rilevata alcuna differenza statisticamente significativa nella dose giornaliera prescritta o nella durata del trattamento tra le persone che hanno tentato il suicidio e quelle esaminate in totale. Tuttavia, 14 pazienti (donne) che avevano tentato il suicidio dopo il trattamento avevano ricevuto 2 o più cicli di trattamento (24%; 13-35%) rispetto alle donne mai ricoverate per tentato suicidio (9%, 8-10%) (p<0,001).
I pazienti con un tentativo di suicidio precedente al trattamento (n=32) non hanno mostrato un aumento delle tendenze suicide durante o dopo il trattamento: 12 di questi pazienti hanno ritentato o compiuto il suicidio durante il follow-up.
Al contrario, dei 14 pazienti con un primo tentativo di suicidio durante o entro sei mesi dalla fine del trattamento, 10 hanno ritentato o compiuto il suicidio durante il follow-up (p=0,034).
Confrontando i tassi relativi all'anno precedente al trattamento (1,66/1000 anni-persona) con il tasso nei sei mesi successivi al trattamento (2,52/1000 anni-persona), la differenza di tasso più elevata è stata correlata ai primi tentativi di suicidio: 0,86 casi per 1000 anni-persona (da -0,78 a 2,50). Per tutti i tentativi, la differenza corrispondente era 0,40 (da -1,46 a 2,26) per 1000 anni-persona.
Alla fine del 2001 sono stati registrati 17 suicidi tra i pazienti maschi (1 durante il trattamento e 2 nell'anno successivo) e 7 tra le donne (0,4%). Il tasso di mortalità standardizzato nei pazienti maschi suicidatisi nell'anno successivo al trattamento era pari a 1,9 (0,4-5,4), mentre nelle pazienti è risultato pari a 1,8 (0,7-3,9) negli 11 anni successivi al trattamento.
Per Giovanni D’AGATA, presidente e fondatore dello “Sportello dei Diritti”, l'aumento del rischio di tentato suicidio nei 6 mesi successivi alla fine del trattamento con isotretinoina potrebbe giustificare un monitoraggio più stretto dei pazienti a rischio di suicidio fino ad un anno dopo la fine del trattamento. [MORE]
(Notizia segnalata da Giovanni D’AGATA)
Redazione
Vuoi restare sempre aggiornato con le notizie più importanti?
Iscriviti ai nostri canali ufficiali:
Riceverai in tempo reale tutti gli aggiornamenti direttamente sul tuo smartphone.